Thủ tướng chỉ đạo giảm bớt quy trình cấp phép vaccine Nanocovax nhưng phải chặt chẽ
(DNTO) - Thủ tướng Chính phủ Phạm Minh Chính yêu cầu Bộ trưởng Bộ Y tế nghiên cứu, chỉ đạo việc cấp phép và sử dụng vaccine Nanocovax theo hướng giảm bớt quy trình, thủ tục hành chính, nhưng phải đảm bảo chặt chẽ theo quy định và thẩm quyền.

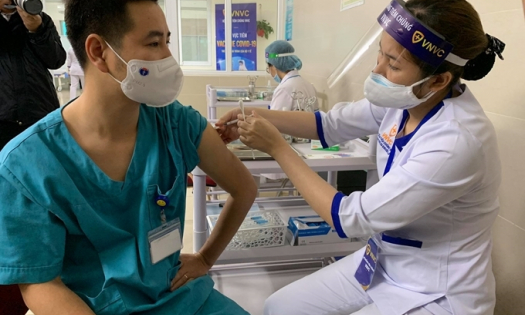
Vaccine Nanocovax. Ảnh: T.L
Văn phòng Chính phủ nhận được văn bản ngày 1/8/2021 của GS.TS Nguyễn Gia Bình, Chủ tịch Hội Hồi sức cấp cứu và chống độc Việt Nam, Ủy viên Hội đồng chuyên môn Ban Bảo vệ chăm sóc sức khỏe Trung ương, kiến nghị về việc cấp phép sử dụng vaccine trong tình huống khẩn cấp.
Về việc này, Thủ tướng Phạm Minh Chính có ý kiến: Đồng chí Bộ trưởng Bộ Y tế nghiên cứu, chỉ đạo việc cấp phép và sử dụng vaccine Nanocovax theo hướng giảm bớt quy trình, thủ tục hành chính, nhưng phải đảm bảo chặt chẽ theo quy định và thẩm quyền.
Vaccine phòng Covid-19 Nanocovax được Công ty Cổ phần Công nghệ sinh học dược Nanogen phát triển từ tháng 5/2020, dựa trên công nghệ protein tái tổ hợp. Vaccine này đã trải qua 2 giai đoạn thử nghiệm lâm sàng, trong đó giai đoạn 1 bắt đầu từ ngày 18/12/2020 và giai đoạn 2 từ ngày 26/2/2021.
Theo TS. Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học, Công nghệ và Đào tạo (Bộ Y tế), vaccine Nanocovax của Công ty Cổ phần Công nghệ sinh học dược Nanogen và Học viện Quân y nghiên cứu đang thử nghiệm lâm sàng giai đoạn 3 và đang thực hiện đánh giá 3 yếu tố, gồm tính an toàn, tính sinh miễn dịch, hiệu lực bảo vệ trên tình nguyện viên Việt Nam từ 18 tuổi trở lên.
Trong đó, giai đoạn 3a tiêm cho 1.000 đối tượng, đánh giá giữa kỳ tính an toàn, tính sinh miễn dịch, tỷ lệ tiêm cho nhóm tình nguyện viên vaccine trên nhóm tiêm giả dược là 6:1. Giai đoạn 3b được tiêm trên 12.000 người, tỷ lệ tiêm cho nhóm tình nguyện viên vaccine trên nhóm tiêm giả dược là 2:1.
Dự kiến, trước ngày 15/8 sẽ có đánh giá kết quả thử nghiệm lâm sàng giai đoạn 3a.
Trên cơ sở này, các cơ quan liên quan sẽ rà soát để có dữ liệu ban đầu về tính sinh miễn dịch và hiệu lực bảo vệ của vaccine của giai đoạn 3a.
Vaccine Covid-19 Covivac an toàn, chuẩn bị thử nghiệm giai đoạn 2
Hiện vaccine thứ hai của Việt Nam là Covivac đã được các chuyên gia đánh giá là vaccine an toàn, sinh miễn dịch tốt, và vaccine này chuẩn bị chuyển sang thử nghiệm giai đoạn 2. Covivac do Viện Vaccine và Sinh phẩm y tế sản xuất. Đây là ứng viên vaccine Covid-19 thứ 2 ở Việt Nam được cấp phép thử nghiệm trên người sau vaccine Nano Covax của Công ty Nanogen.
Ở giai đoạn 1, Covivac tiêm thử nghiệm trên 120 tình nguyện viên chia làm 4 nhóm và 4 liều khác nhau, 20 người tiêm giả dược.
Viện Vệ sinh dịch tễ Trung ương đánh giá, cả 4 nhóm đều an toàn và dung nạp tốt. Quá trình tiêm chỉ ghi nhận một số ít bị đau nhẹ chỗ tiêm, ngoài ra tất cả các phản ứng khác đều ở mức độ nhẹ và thường hết sau 30 phút.
Về miễn dịch, 4 nhóm tiêm vaccine Covivac đều sinh miễn dịch, có nhóm chuyển đổi huyết thanh tăng 10 lần so với trước khi tiêm.
Đơn vị nghiên cứu là Viện Vaccine và Sinh phẩm Y tế, Bộ Y tế (Ivac) sẽ đề xuất liều chuyển tiếp 3 mcg cho giai đoạn 2. Ngoài ra, giai đoạn này Ivac cũng sẽ bổ sung thêm 1 liều trung gian giữa 3 mcg và 10 mcg.
Kết quả thực hiện các nghiên cứu tiền lâm sàng của Covivac tại Ấn Độ, Mỹ và Việt Nam cho thấy tính an toàn và hiệu quả trên thực nghiệm. Các đánh giá tiền lâm sàng cho thấy, vaccine đáp ứng miễn dịch tốt, an toàn, hiệu quả ngăn ngừa biến thể của Anh và Nam Phi.
Giai đoạn tiền lâm sàng cũng chứng minh vaccine Covivac mang nhiều ưu điểm như tính sinh miễn dịch cao, phù hợp với cơ sở vật chất của các cơ sở tiêm chủng tại Việt Nam, cũng như phù hợp với biến chủng của virus SARS-CoV-2.