Tiếp tục đề nghị bổ sung dữ liệu về hiệu quả bảo vệ của vaccine Nanocovax
(DNTO) - Chiều 20/12, Bộ Y tế thông tin về kết luận cuộc họp xem xét báo cáo cập nhật, bổ sung kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 vaccine Nanocovax của Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia.
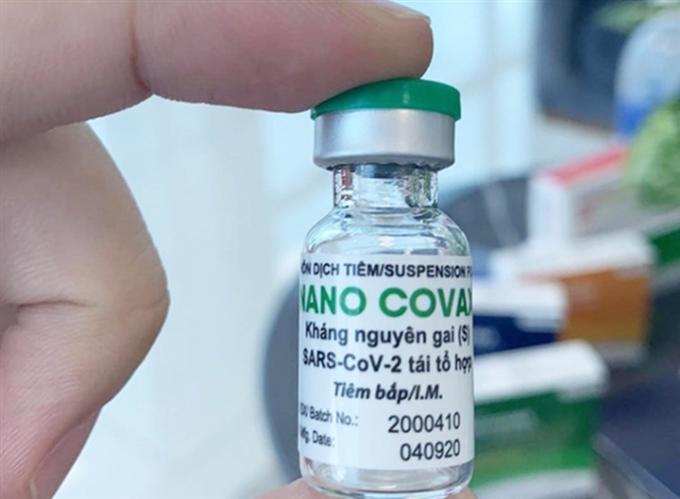
Vaccine Covid-19 Nanocovax đạt yêu cầu về tính sinh miễn dịch theo hướng dẫn chuyên môn về xem xét tính an toàn và hiệu quả bảo vệ phục vụ đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 của vaccine ngừa Covid-19 sản xuất trong nước. Ảnh: T.L
Trên cơ sở báo cáo, ý kiến của các thành viên hội đồng, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia thống nhất kết luận: Vaccine Covid-19 Nanocovax đạt yêu cầu về tính sinh miễn dịch theo hướng dẫn chuyên môn về xem xét tính an toàn và hiệu quả bảo vệ phục vụ đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 của vaccine ngừa Covid-19 sản xuất trong nước (ban hành kèm theo Quyết định 5259/QĐ-BYT ngày 11/11/2021 của Bộ trưởng Bộ Y tế) dựa trên dữ liệu báo cáo bổ sung giữa kỳ phiên bản 8.0 ngày 30/11/2021.
Về hiệu quả bảo vệ của vaccine, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia thống nhất cần tiếp tục bổ sung dữ liệu các trường hợp mắc Covid-19 theo đề cương nghiên cứu đã được phê duyệt. Chấp nhận đề xuất của tổ chức nhận thử (Học viện Quân Y, Viện Pasteur TPHCM) và nhà tài trợ (Công ty cổ phần Công nghệ sinh học dược Nanogen) về việc xác minh các trường hợp mắc Covid-19 trong nghiên cứu tính đến hết ngày 13/12/2021 làm dữ liệu chính thức để phân tích, đánh giá hiệu lực bảo vệ trực tiếp của vaccine ngừa Covid-19 Nanocovax.
Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia thống nhất đề nghị tổ chức nhận thử hoàn thiện báo cáo và gửi báo cáo phân tích hiệu lực bảo vệ trực tiếp của vaccine về hội đồng trước 15h00 ngày 22/12/2021 để xem xét, đánh giá.
Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia ghi nhận và đánh giá cao sự đóng góp của người tình nguyện tham gia nghiên cứu thử nghiệm lâm sàng vaccine ngừa Covid-19 nói chung, vaccine Covid-19 Nanocovax nói riêng.
Đến nay, nghiên cứu thử nghiệm lâm sàng vaccine ngừa Covid-19 Nanocovax đã có đủ dữ liệu để đánh giá hiệu quả bảo vệ của vaccine. Để bảo vệ cho người tình nguyện tham gia nghiên cứu, đặc biệt những người tình nguyện được tiêm giả dược, hội đồng chấp nhận đề xuất của tổ chức nhận thử và nhà tài trợ về việc "mở mù" để tiêm vaccine Covid-19 được Bộ Y tế cấp phép lưu hành cho người tình nguyện tham gia nghiên cứu ở nhóm sử dụng giả dược.
Được biết, trong nghiên cứu này thực hiện "làm mù" để đảm bảo tính khách quan, theo đó người tình nguyện tham gia nghiên cứu được quản lý bằng mã số và được phân một cách ngẫu nhiên vào nhóm tiêm vaccine nghiên cứu hoặc nhóm tiêm giả dược.