Bộ Y tế lần đầu lên tiếng sau vụ Công ty Việt Á 'thổi giá' kit test Covid-19
(DNTO) - Chiều 21/12, Bộ Y tế phát thông tin khẳng định thực hiện đúng quy định trong cấp phép và bảo đảm chất lượng các sinh phẩm xét nghiệm Covid-19. Đồng thời nhấn mạnh: Việc nâng khống giá bộ xét nghiệm Covid-19 của Công ty cổ phần Công nghệ Việt Á là rất nghiêm trọng, cần phải được xử lý nghiêm minh.

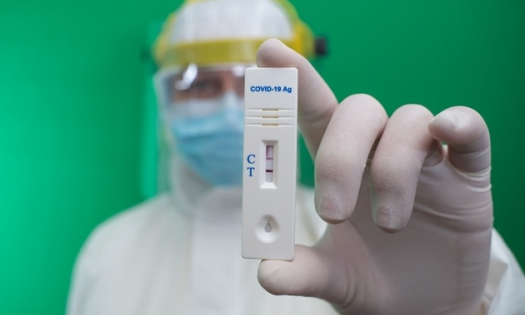
Cán bộ y tế lấy mẫu xét nghiệm Covid-19. Ảnh: T.L
Bộ Y tế khẳng định thực hiện đúng quy định trong cấp phép lưu hành sinh phẩm xét nghiệm của Công ty cổ phần Công nghệ Việt Á. "Việc cấp phép này đã đảm bảo đáp ứng nhu cầu xét nghiệm tại thời điểm rất khó khăn khi tiếp cận với nguồn cung ứng sinh phẩm trên thế giới", Bộ này nhấn mạnh.
Đến ngày 4/12/2020, Bộ Y tế đã có Quyết định số 5071 cấp phép lưu hành 5 năm đối với bộ sinh phẩm xét nghiệm SARS-CoV-2 chủng loại LightPoweriVA SARS-CoV-2 1st RT-rPCR Kit của Công ty cổ phần Công nghệ Việt Á. Cũng tại Quyết định trên, Bộ Y tế cấp phép lưu hành cho sinh phẩm xét nghiệm SARS-CoV-2 chủng loại One-Step RT- PCR Covid-19 Kit Thai Duong Multiplex-3 target genes Version 1.0 của Công ty cổ phần Sao Thái Dương.
Theo Bộ Y tế, tính đến ngày 20/12/2021, Bộ Y tế đã cấp phép 146 sinh phẩm xét nghiệm SARS-CoV-2, trong đó có 46 sinh phẩm xét nghiệm vật liệu di truyền (PCR, LAMP) tương tự như sản phẩm của Công ty cổ phần Công nghệ Việt Á và Công ty cổ phần Sao Thái Dương (bao gồm 7 sinh phẩm sản xuất trong nước và 39 sinh phẩm nhập khẩu). Bộ Y tế xác định việc cấp phép cho nhiều sản phẩm là để tăng cường nội địa hóa, chủ động nguồn cung và tạo sự cạnh tranh về giá sinh phẩm xét nghiệm.
Tất cả các sản phẩm cấp phép đều đã được đánh giá đạt yêu cầu, đáp ứng tiêu chuẩn, chất lượng của Việt Nam và đảm bảo đúng theo các quy định hiện hành. Các sản phẩm sau khi được cấp phép đều được theo dõi chất lượng và tính ổn định.
Bộ Y tế nói gì về việc WHO không chấp nhận kit test của Công ty Việt Á?
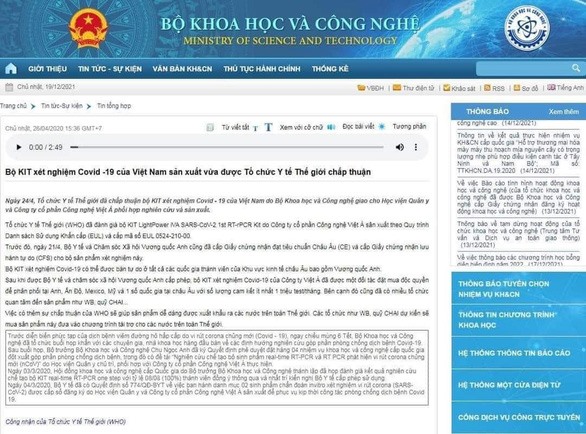
Thông tin về kit test của Việt Á được WHO chấp thuận từng đăng trên website Bộ KHCN. Ảnh: T.L
Trước đó, vào ngày 25/4/2020, Bộ Khoa học- Công nghệ thông tin chính thức bằng thông cáo báo chí về việc bộ kit xét nghiệm của công ty Việt Á được WHO chấp thuận với mã số EUL 0524‐210‐00.
Tuy nhiên, sau đó WHO đưa ra kết luận: Bộ xét nghiệm LightPower iVASARS-CoV-2 1stRT-rPCR Kit với mã sản phẩm VA.A02-055H, sản xuất bởi Công ty cổ phần công nghệ Việt Á, địa chỉ 372A/8 Hồ Văn Huê, phường 9, quận Phú Nhuận, TP.HCM không đủ điều kiện để vào chương trình mua sắm của WHO.
Sau khi ông Phan Quốc Việt, Chủ tịch HĐQT kiêm Tổng giám đốc Công ty Cổ phần công nghệ Việt Á, bị khởi tố với cáo buộc nâng khống giá kit xét nghiệm Covid-19, những thông tin đăng tải trên website của Bộ Khoa học- công nghệ công bố "đánh giá của Tổ chức Y tế thế giới" và "Bộ Y tế Anh cấp chứng nhận đạt chuẩn châu Âu" cho bộ kit test của Công ty Việt Á đã bị gỡ.
Liên quan đến câu chuyện vì sao WHO không chấp nhận kit test của Công ty Việt Á, trong thông tin gửi báo chí chiều 21/12, Bộ Y tế giải thích rằng: Về danh mục các sinh phẩm do Tổ chức Y tế thế giới (WHO) công bố và đưa vào danh sách sử dụng khẩn cấp (EUL), các công ty mong muốn sản phẩm của mình được đưa vào danh sách của WHO thì nộp hồ sơ đề nghị WHO xem xét. Tuy nhiên, mỗi quốc gia, tổ chức đều xây dựng tiêu chí và yêu cầu về hồ sơ, sản phẩm khác nhau về việc chấp thuận lưu hành sinh phẩm. Các công ty có nhu cầu lưu hành, sử dụng tại quốc gia và tổ chức nào sẽ nộp hồ sơ theo quy định của từng tổ chức, quốc gia đó.
Do vậy, việc cấp phép của Bộ Y tế đối với sản phẩm của Công ty cổ phần Công nghệ Việt Á và các nhà sản xuất khác không phụ thuộc vào danh sách do WHO công bố. Tính đến nay, đối với sinh phẩm xét nghiệm PCR, theo danh sách EUL của WHO có 23 sản phẩm được phê duyệt; trong khi đó, tại Châu Âu đã chấp thuận 589 loại sinh phẩm, Mỹ chấp thuận sử dụng 276 loại sinh phẩm, Hàn Quốc chấp thuận sử dụng trong nước 31 sinh phẩm...
Giá sinh phẩm xét nghiệm phải thông qua đấu thầu công khai
Trong thông báo gửi báo chí chiều nay, Bộ Y tế cho rẳng, giá sinh phẩm xét nghiệm phải thông qua đấu thầu công khai, minh bạch. Theo quy định của Luật giá, trang thiết bị y tế và sinh phẩm xét nghiệm không thuộc trong danh mục mặt hàng phải quản lý giá. Giá trang thiết bị y tế và sinh phẩm xét nghiệm được xác định thông qua đấu thầu và giá các sản phẩm khác nhau theo từng thời điểm và số lượng mua sắm, khả năng cung ứng.
Bộ Y tế đã hướng dẫn, đôn đốc, yêu cầu các doanh nghiệp cung ứng trên thị trường triển khai thực hiện việc công khai giá trang thiết bị y tế và công khai kết quả trúng thầu. Hiện tại, trên Cổng công khai giá trang thiết bị y tế đã có trên 1.600 doanh nghiệp thực hiện công khai giá bán (giá niêm yết theo quy định của Luật giá), có trên 60.000 mặt hàng trang thiết bị y tế công khai giá (8.256 thiết bị y tế; 36.191 vật tư y tế; 15.584 IVD) và 93.253 kết quả trúng thầu.
Cùng thời điểm Công ty cổ phần Công nghệ Việt Á niêm yết giá trên Cổng công khai giá là 470.000 đồng/sản phẩm, thì Công ty cổ phần Sao Thái Dương niêm yết giá loại xét nghiệm PCR là 300.000 đồng/sản phẩm và xét nghiệm LAMP có giá 385.000 đồng/sản phẩm, Công ty Ampharco U.S.A có giá 179.800 đồng/sản phẩm; có 15 sản phẩm PCR nhập khẩu đã được cấp phép đăng ký và niêm yết giá từ 280.000 đồng đến 600.000 đồng/sản phẩm. Thông tin này đã được công khai trên Cổng công khai giá để các địa phương, cơ sở y tế nắm bắt, tham khảo khi xây dựng kế hoạch và thực hiện mua sắm, đấu thầu, sử dụng sản phẩm phục vụ nhu cầu phòng, chống dịch, mà không phải là giá bắt buộc áp dụng. Các địa phương, đơn vị thực hiện mua sắm, đấu thầu theo đúng quy định và chịu trách nhiệm về kết quả thực hiện.
Bộ Y tế đã có nhiều văn bản yêu cầu các nhà cung cấp, kinh doanh trang thiết bị y tế thực hiện nghiêm việc công khai, cập nhật về giá trang thiết bị y tế bảo đảm chính xác và đầy đủ các thông tin liên quan đến hàng hóa theo quy định, trong đó đề nghị công khai giá bán đến đơn vị nhỏ nhất (Ví dụ: đối với trang thiết bị y tế chẩn đoán in vitro, đề nghị công khai giá đến 01 đơn vị xét nghiệm). Trong trường hợp bất khả kháng có biến động về giá (nếu có) do ảnh hưởng của dịch bệnh, đề nghị các đơn vị chủ động rà soát, cập nhật và chịu trách nhiệm về giá niêm yết trên Cổng điện tử công khai giá.
Ngoài ra, Bộ Y tế thực hiện nhiều biện pháp để đảm bảo nguồn cung và giảm giá, trong đó tập trung ưu tiên đẩy mạnh việc cấp giấy phép nhập khẩu và sản xuất trong nước để tăng số lượng mặt hàng cung ứng trên thị trường, nhằm tăng sự cạnh tranh, giảm giá sản phẩm. Mặt khác, Bộ Y tế cũng đã hướng dẫn các đơn vị, địa phương gộp mẫu 10, 15 cho 1 xét nghiệm PCR để giảm chi phí xét nghiệm...
Trước đó, ông Phan Quốc Việt (41 tuổi), Tổng giám đốc Công ty Việt Á, cùng nhiều thuộc cấp đã bị Bộ Công an khởi tố, điều tra về hành vi “thổi giá” kit xét nghiệm Covid-19. Công ty Việt Á quảng cáo đây là bộ kit chẩn đoán SARS-CoV-2 đầu tiên tại Việt Nam, được Bộ Y tế cấp số đăng ký; Bộ Y tế và Chăm sóc xã hội Anh cấp giấy chứng nhận đạt tiêu chuẩn châu Âu (CE), cấp giấy chứng nhận lưu hành tự do (CFS); WHO cấp chứng nhận chất lượng sản phẩm cho phép lưu hành toàn cầu. Cũng theo quảng bá, năng lực sản xuất của công ty khoảng 30.000 kit xét nghiệm/ngày. Bộ kit xét nghiệm này cho kết quả chính xác 100% sau 2 giờ và đáp ứng được các tiêu chí tương đương các bộ sinh phẩm do CDC Mỹ và WHO hướng dẫn.